【色谱分离技术】
拼译:technique of chromatographic seperation
色谱学已有80年的历史,而在实验室中作为工具使用开始于30年代初。从60年代末到现在,色谱分离技术广泛用于有机化学、生物化学、药物学和环保学等而倍受重视。1952年英国Martin和Synge因发展了分配色谱而获得诺贝尔奖。此外,色谱分离技术在一些获得诺贝尔奖项目中起着关键的作用。例如:1937年类胡萝卜素化学、维生索A和B,1950年性激素化学及其分离,肾皮素化学及其分离,1958年胰岛素结构测定,1972年核糖核酸化学酶结构的研究都使用了色谱分离方法。
色谱法是一种以分配平衡为基础的分离方法,在所有分离技术中它具有快速、简便、纯度高等优点。有机化学家用此技术进行分离、纯化所合成的产物和中间体,该法是目前认为最有效的方法,特别是对天然物主要化学成分的微量分离、微量合成产物的分离,或一些立体异构的分离,样品往往只有几十毫克到几百毫克,用常规的方法是无法达到分离纯化的目的。现代液相色谱有液-固,液-液,离子交换和凝胶渗透四种不同类型,其中液-固色谱是用得最多的一种。从操作方式看,液-固色谱又分为洗脱法,前沿法和取代法。目前高效液相色谱(HPLC)主要采用洗脱法。近年来,前沿法也开始受到重视。制备型高效液相色谱(HPLC) 制备型高效液相色谱是近年发展起来的新颖快速分离技术,它的分离速度比经典的液相柱层析法快上百倍。在色谱分离技术中,要求在尽可能短的时间内以最大的分辨率,将混合样品中各组分分开,关键是做到色谱分离条件的优化,以达到最佳柱效和最有效的分离的目的。制备色谱的几个关键技术是:(1)色谱柱的选择;一种为半制备柱,内径9~10mm,长250~500mm,填料常用硅胶或氧化铝,其粒度直径是5~10μm,柱效可达到15000左右,每次注入样品5~10mg,这种柱适于微量样品的分离。一般用的制备柱内径20~22mm,长250mm,装入较粗的填料(20~30μm),这种柱的柱效较低,但样品处理量大。(2)对色谱仪部件的要求:高压输液泵一般流量为30~100ml/min,工作压力为100kg/min。进样器的样品环管要细而长,检测器要求线性响应范围宽,最常用的是示差折光检测器,馏分收集器可用手动或微处理机控制收集冈一个色谱峰的纯组分。(3)每个色谱柱的容量有限,当不断增加进样量时会使色谱分离度变差,可切割部分未充分分离的色谱峰,用TLC检查其纯度,然后确定是否需进一步分离。为解决由于样品过载使原来可以分开的色谱峰重叠,可采用串连延长色谱柱或再循环的办法,后者通过一个四通阀将柱流出液再导入色谱柱再次进行分离,循环4~5次为限,每次可提高柱效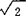 倍。对于一些复杂的生化样品,分离纯化所遇到的难题,也是采用色谱峰分段切割的方法,从中取得某些纯组分。(4)进样前的准备工作,粗产物要用适当方法加以精制。洗脱液通常采用石油醚(30~60℃)与乙酸乙酯按一定比例配成的混合溶剂,其配比大小最好先用薄层色谱(TLC)试验来调节洗脱液的极性大小。溶液也要事先过滤才进入仪器。制备型超临界流体色谱(SFC) 近年来,制备型洗脱色谱又有了新的发展,称为制备型超临界流体色谱(Preparative Supercritical Fluid Chromatography),简称SFC。它所用的仪器设计,包括分析填充柱都与HPLC相似,唯一不同是馏分的收集方式更完善,可以在常压、高压下用溶剂洗脱吸附在固定相上的官能团化合物,并直接把它们从洗脱液中分离出来得到纯组分。这样,制备SFC成为分离技术中一个相对容易和有用的工具。它可以小规模制备纯产物在10-3~1g,用于天然产物的结构分析或分离鉴定微量合成的有机产物。这种色谱的应用范围比气相色谱(GC)宽,(扩大到重化合物),操作时间比HPLC短,特别是用减压的方法令洗脱液与产物分离而得到纯组分,使制备SFC成为一个分级分离的定量方法。大规模的制备SFC样品处理量在1g/h~1kg/h,它可作为最终纯化产品方法或把化学合成的和天然物分级分离方法向着工业化发展,看来是很有前途的,因为它不像GC,不能处理重的和热不稳定化合物,也不像制备HPLC,产物要从溶剂中回收,而是直接可用于试验、反应或其它用途。因此,到了80年代,SFC作为一种分析工具对GC和HPLC的补充,而制备SFC则以生产规模跟现代制备HPLC正在平行发展中。快速柱层析技术(Preparative Rapid Chromatographic Technique) 经典的柱层析技术由于分离速度慢而曾一度减低了人们对它的兴趣。然而,70年代后期发展起来的快速柱层析技术已成为一种常规分离纯化方法而深受有机化学工作者欢迎。它的特点是用短柱,在洗脱时用压缩空气在柱上端加中等压力,使洗脱液流速在5cm/min左右。用硅胶60作柱填充剂,粒度为70~230目,用量一般是样品重的20~50倍,床高13~16cm。洗脱液用乙酸乙酯和己烷(或30~60°的石油醚)的混合溶剂,这样可把在TLC上△Rf≥0.15的两个混合组分分开,达到中等的分辨率。通常0.01g~10g样品分离可在10~15min内完成。分离技术的关键在选用不同直径大小的色谱柱时要视样品量而定,样品量愈多,柱直径要愈大。此外混合溶剂配比(即洗脱液的极性)要由混合组分的△Rf值来决定,因此,在样品分离前需在薄层硅胶板上点样,然后在适当配比的混合溶剂中展开,计算出△Rf值后确定洗脱液的配比及色谱柱直径的大小。收集洗脱出来的每个馏分体积大小也由样品量而定。由于应用中各种样品结构性质各异,需在实践中摸索出最佳条件。例如:200mg的苄醇纯化的标准条件是用40~63μm粒度的硅胶60装入直径20mm的色谱柱,床高15cm,洗脱液是25%的乙酸乙酯/石油醚混合溶剂。快速柱色谱分离技术是目前公认的最经济而简便的分离纯化方法,样品回收率在95%以上。此方法将更为广泛地应用在有机合成、药物合成和天然物研究等各个领域。【参考文献】:1 Clark W S,et al.J Org Chem,1978,43(14)∶29232 SnyderL R,et al.Indroduction to Modern Liquid Chromatography 2nd ed,19793 谢光华,等.现代液相色谱,19894 Derek A H.J of Chromatography,1990,523∶11~215 Berger C,et al.J of Chromatography,1990,505∶37~436 Matsuta R,et al.Chromatographia,1991,32(5/6);233~2377 李淑琏.化学通报,1991,5∶28~30
倍。对于一些复杂的生化样品,分离纯化所遇到的难题,也是采用色谱峰分段切割的方法,从中取得某些纯组分。(4)进样前的准备工作,粗产物要用适当方法加以精制。洗脱液通常采用石油醚(30~60℃)与乙酸乙酯按一定比例配成的混合溶剂,其配比大小最好先用薄层色谱(TLC)试验来调节洗脱液的极性大小。溶液也要事先过滤才进入仪器。制备型超临界流体色谱(SFC) 近年来,制备型洗脱色谱又有了新的发展,称为制备型超临界流体色谱(Preparative Supercritical Fluid Chromatography),简称SFC。它所用的仪器设计,包括分析填充柱都与HPLC相似,唯一不同是馏分的收集方式更完善,可以在常压、高压下用溶剂洗脱吸附在固定相上的官能团化合物,并直接把它们从洗脱液中分离出来得到纯组分。这样,制备SFC成为分离技术中一个相对容易和有用的工具。它可以小规模制备纯产物在10-3~1g,用于天然产物的结构分析或分离鉴定微量合成的有机产物。这种色谱的应用范围比气相色谱(GC)宽,(扩大到重化合物),操作时间比HPLC短,特别是用减压的方法令洗脱液与产物分离而得到纯组分,使制备SFC成为一个分级分离的定量方法。大规模的制备SFC样品处理量在1g/h~1kg/h,它可作为最终纯化产品方法或把化学合成的和天然物分级分离方法向着工业化发展,看来是很有前途的,因为它不像GC,不能处理重的和热不稳定化合物,也不像制备HPLC,产物要从溶剂中回收,而是直接可用于试验、反应或其它用途。因此,到了80年代,SFC作为一种分析工具对GC和HPLC的补充,而制备SFC则以生产规模跟现代制备HPLC正在平行发展中。快速柱层析技术(Preparative Rapid Chromatographic Technique) 经典的柱层析技术由于分离速度慢而曾一度减低了人们对它的兴趣。然而,70年代后期发展起来的快速柱层析技术已成为一种常规分离纯化方法而深受有机化学工作者欢迎。它的特点是用短柱,在洗脱时用压缩空气在柱上端加中等压力,使洗脱液流速在5cm/min左右。用硅胶60作柱填充剂,粒度为70~230目,用量一般是样品重的20~50倍,床高13~16cm。洗脱液用乙酸乙酯和己烷(或30~60°的石油醚)的混合溶剂,这样可把在TLC上△Rf≥0.15的两个混合组分分开,达到中等的分辨率。通常0.01g~10g样品分离可在10~15min内完成。分离技术的关键在选用不同直径大小的色谱柱时要视样品量而定,样品量愈多,柱直径要愈大。此外混合溶剂配比(即洗脱液的极性)要由混合组分的△Rf值来决定,因此,在样品分离前需在薄层硅胶板上点样,然后在适当配比的混合溶剂中展开,计算出△Rf值后确定洗脱液的配比及色谱柱直径的大小。收集洗脱出来的每个馏分体积大小也由样品量而定。由于应用中各种样品结构性质各异,需在实践中摸索出最佳条件。例如:200mg的苄醇纯化的标准条件是用40~63μm粒度的硅胶60装入直径20mm的色谱柱,床高15cm,洗脱液是25%的乙酸乙酯/石油醚混合溶剂。快速柱色谱分离技术是目前公认的最经济而简便的分离纯化方法,样品回收率在95%以上。此方法将更为广泛地应用在有机合成、药物合成和天然物研究等各个领域。【参考文献】:1 Clark W S,et al.J Org Chem,1978,43(14)∶29232 SnyderL R,et al.Indroduction to Modern Liquid Chromatography 2nd ed,19793 谢光华,等.现代液相色谱,19894 Derek A H.J of Chromatography,1990,523∶11~215 Berger C,et al.J of Chromatography,1990,505∶37~436 Matsuta R,et al.Chromatographia,1991,32(5/6);233~2377 李淑琏.化学通报,1991,5∶28~30(华南师范大学李淑琏教授撰)