【高分子凝胶的体积相变】
高分子凝胶是由高分子的三维网络与溶液组成的多无体系,是自然界中普遍存在的着的一种物质形态,生物机体的许多部分就是由凝胶构成的,眼球就是一个例子。高分子形成三维网络结构有两种方式,即物理交联和化学交联。前者是分子链通过缠结点、微晶区等物理结合形成三维网络,这些交联点随温度等外界条件而变化,会出现溶胶-凝胶转变。而化学交联是分子链靠共价汽键式配合键结合,产生三维网络结构。早在40多年前,P,T.Floryt和W.T.Stochmayer就研究了电解溶质凝胶的空胀现象70年代末,由于T.Tonaka等人发现了凝胶的体积相度现象,促进了该领域的发展1980年,F.Tonaka等人发现化学交联的部分水解聚丙烯酰胺凝胶在水/丙酮混合溶液中。其溶胀体积随丙酮浓度的增加而减小,当丙酮达到某一浓度时,这种体积变化表现为不连续的跃迁式,他们称之为体积相变。研究发现水解程度不同的凝胶,出现体积相变的丙酮浓度不同,相变中体积变化的大小亦不相同。他们提出体积相变是平衡的热力学一级相变。
凝胶的体积之所以溶胀或收缩,是由于凝胶内部的溶液与其周围的溶液之间存在着渗透压π。π与溶剂的化学位Δμ0有如下关系:π=-Δμ/V0 (1)
V0是溶剂的摩尔体积。根据Flory理论,Δμ0中有来自3个方面的贡献,即高分子与溶剂混合的Δμ0,mix,电质凝胶中的可迁移离子引起的Δμ0,ion以及溶胀导致高分子网络形所伴随的Δμ0,ela,所以Δμ0=Δμ0,mix+Δμ0,ion+Δμ0,ela (2)
Δμ0,mix可以经典的Flory-Huggins格子模型计算,当分子量无限大时,Δμ0,mix=RT[ln(1-Φ)+Φ+XΦ2] (3)
R和T分别为常数和绝对温度,x是Flory相互作用函数。
高分子电解质凝胶中有可迁移的反离子存在,为满足电中性的条件,它们不能自由地扩散到凝胶外部的溶液中去。凝胶就象-个反离子不能通过的半透膜,在其两侧会产生渗透压。如果忽略固定于高分子网络上的电离基团间以及它们与反离子的相互作用,当可迁移离子在凝胶中和外部溶液中的浓度分别为c和c′(mol·cm-3)时,Δμ0,ion=-RTV0(c-c′) (4)
如果溶液中有添加盐,c与c′的关系按Don-nan平衡条件计算;无添加盐时c′=0。设不含溶液的干凝胶中有效高分子链密度为v(mol·cm-3),每个有效链带有f个一价电离基,反离子也是一从价,则:Δμ0,ion=-RTV0fvΦ (5)
凝胶溶胀时高分子网络受到拉伸,导致覆盖象熵减小,由理想橡胶仿射(affine)网络的弹性理论可得:
将(3)、(5)、(6)式代入(2)式,或得凝胶的渗透压为:
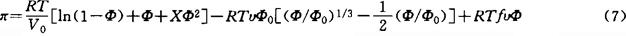
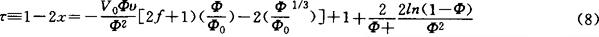
τ称为换算温度,它反映了溶液对高分子的特性,良溶剂时τ>0,贫溶剂时τ<0。
T.Tanaka等人(1980)利用(8)式计算凝胶的理论溶胀曲线。对聚丙烯酰胺来说,水是良溶剂而丙酮是贫溶剂,τ增大相当于丙酮浓度下降。在τ>0的区域,无论电离基团密度f取何值,凝胶溶胀(Φ/Φ0<1),体积随τ连续变化(实线。当τ<0时f<0.659为临界值,f<0.659时体积连续变化;f>0.659时则会-在某个τ处出现体积相变。研究表明,体积相变是凝胶态物质的普遍现象。为了从物质特性来描述体积相变现象,E.L.Cussler等人(1990)发展了高分子溶液的格子流体理论,提出了可溶液的格子流体理论,提出了可压缩格子模型,试图将凝胶的相图与对应的未交联高分子的溶液相图联系起来。J.M.Puausnitz等人(1989,1990)则通过在配分函数中引进氢键的相互作用能,建立了水凝胶的状态方程。然而,这些理论都只是对(3)式中的Floy相互作用函数x作些改良。而对电解质凝胶来说,电离基之间的相互作用起着重要的角色,C.KoňdK和R.Bansil(1990)在凝胶状态方程中用DebyeHückel理论来描述这种相互作用。童真还发现凝胶中的电离基密度f对其剪切模量有很大的影响,这表明电离基团的存在改变了分子链的构象,从而偏离理想的橡胶的弹性行为。从上述理论可知,凝胶体系的特性是由x、f、v3个因素来决定的,凡是可以改变这3个参数的变化,都可能影响体积相变。下面介绍一些溶液组成以外的因素。1984年,Y.Hirokawa和T.J.Tanaka报告了不带电荷的聚N-异取代丙基同丙烯酰胺凝胶(PNIPA)在纯水中的体积相变的现象。1990年H.Inomata等人研究了具有不同N-取代丙基的聚丙烯酰胺凝胶的相图。当N-取代基分别为环丙基(NCPA)、异丙基(NIPA)、正丙基(NNPA)时,丙基的空间体积依次增大,高分子网络的疏水性增强,使得发生体积相变的温度也依此顺序下降。其中聚NCPA凝胶中疏水基(环丙基)的体积量小,所以没有观察体积相变。据此,他们认为疏水性相互作用是造成低温溶胀、高温收缩型体积的主要原因。没有找到描述此种相互作用的理论。在凝胶的高分子网络上可以引入强电离基团(如磺酸基)或弱电离基团(如羧酸基),笔者的结果表明,H+浓度的变化不会改变强电解质凝胶的溶胀特性,但对弱电解质凝胶的溶胀由有很大的影响(童真等,1992)。这是由于H+浓度的变化引起弱电解质凝胶中电荷密度f发生变化,从而改变凝胶的渗透压。是Tanaka等人最早报告了由H+浓度变化引起部分水解的聚丙烯酰胺凝胶发生体积相变的发现。I.O.hmine和Tanaka(1982)实验还发现添加盐的金属阳离子价态对荷电凝胶的体积相变有很大影响。他们认为凝胶内部电中性的要求使得反离子价数增高时,其浓度C就必须降低,由(4)式可知这会导致π减少引起体积收缩。他们还试图以此来说明Ca2+离子与生体肌肉的关联。1991年,和田直纯等人报告了一个有趣的结果。他们通过自由基共聚制得了同时带有负电荷基团2-丙烯酰胺基-2-甲基丙磺酸钠(AMPSNa)与电荷革团N-(3-二甲基胺)丙基丙烯酰胺(NDAPA)PNIPA,其中电离基团对单体的总摩尔分数为0.01。该凝胶的体积随温度的变化与单纯的PNIPA凝胶一样,仍属于低温溶胀高温收缩型。将这种两性凝胶发生体积相变的温度对负、正电离基摩尔比(AMPANa/NDAPA)作图1的实践。由图可知,无论哪一种电荷过量,净过量电离基的反离子都会引起渗透压升高,结果相变温度也升高,值得注意的是50/50的凝胶,尽管相变温度(35℃)最低,但仍高于不带电荷的PNIPS的33.2℃,溶胀曲线的形状也不同。这说明虽然高分子网络上电荷的代数和为零,但电离基团之间的正负电荷协同相互仍影响着高分子链的行为,这对认识两性蛋白质的功能很有启发。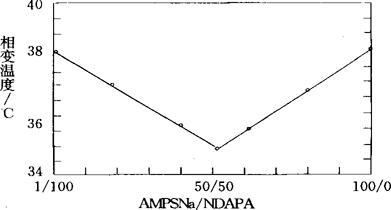

图2
除了通过生化反应改变溶液组成来控制体积相变外,他们还利用酶催化反应来改变溶液的H+浓度、反离子浓度从而控制体积相变(E.Kiokufuta等,1991)。这些结果表明,通过凝胶的体积相变,可以将生化反应产生的化学能反应转换成机械能输出,还可利用酶的选择性,赋予凝胶对特定的分子作出响应能力。凝胶体系的应用是非常广泛的,而且上述各种引起体积相变的因素又可以成为控制凝胶的手段,这就进一步拓宽了凝胶的应用领域。最理想的投药方式应该是在需要的时该、以合适的速率、将所需剂量的药物投到人体需要部位。这种给药需剂量的药物称为DDS,包括控制释放和目标药物。高分子凝胶在环境的刺激下溶胀或收缩,可以改变包理于其中的药物向外扩散的速率,实现药物控制释放。Y.H.Bae等人(1987)研究了在磷酸盐缓冲溶液中消炎痛从PNIPA凝胶中放出的过程。在30℃时消炎痛的释放速率为零,而当温度活跃降至20℃时,立即有消炎痛释出,可见其温度控制脉冲型释放。释放一般有压榨式和皮壳式两种机理,前者随温度升高凝胶体积收缩,将其内部的溶液(水和药物)一起挤压出现来;后者则温度升高凝胶表面迅速收缩,形成致密的表皮层,使其内部的溶液更加难以扩散出来。还有控制胰岛素释放的研究(K.Inhihara等,1988)。将葡萄氧化酶)GOD)与甲基丙烯酸(二乙基胺)乙酯凝胶的一起制成复合膜,用做胰岛素的胶囊。当外输送的葡萄糖浓度升高时,糖GOD的作用下氧化成葡萄酸,于是膜中的H+浓度下降,高分子网络上的正氮离子增多,结果造成凝胶溶胀,胰岛素大量释放。所以特定的物质可以控制药物的释放。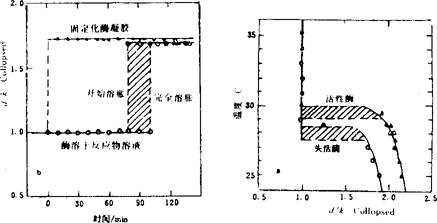
图2
将化学能转变成机械能的换能材料。这种功能将称为chemomechanics,是能够直接将化学能转变成机械能的材料,因此也是一仿生材料。这种材料的设计原则是将高分子网络在外界刺激下发生的微观的构象变化转变成宏观的材料整体的机械运动。利用这种特性可以开发人工肌肉、促动器等。早在40年代末期,W.Kuhn,A.Datchalsky就开始了以凝胶为换能材料的“化学发动机”的研究,到了60年代,人工肌肉的收缩力等指标已接近动物肌肉的水平。铃木等人用反处处冷冻解法制出了聚乙烯醇/聚丙烯酸/聚烯丙基胺凝胶薄膜。改变溶液组成,凝胶体积随之变化,驱动荷重,实现化学能向机械能的直接转换。经33次冷冻、解冻厚度为10μm薄膜,当荷重为1.4kg·cm-2时,响应时间为0.12s,输出能量密度为0.106W·cm-3,与动物肌肉相近。Shiga等人发现对浸泡在电解质溶液中的丙烯酸钠/丙烯酰胺共聚凝胶施加电场时,尽管凝胶没有与电极接触,但仍发生了变形,且与和因真纯等1991年报道的现象不同。他们利用该现象制作了人工手指、人造鱼等样品。除此之外,还有温差、H+浓度等驱动方式,所产生的机械能也不局限于直接以能量的形式输出,还可以转换成材料其它形式的响应。用电场控制过滤膜的孔就是这方面的一个例子。物质分离材料。作为物质分离用材料,凝胶早已广泛地服务于各种液相色谱中了。Cussler等人报告了利用热敏型PNIPA凝胶浓缩溶液的方法。他们先把收缩了的凝胶投入溶液中,在低温T.凝胶溶胀而吸收溶剂然后通过滤分离出浓缩后的溶液。再将吸收了溶剂的凝胶加热,超过相变温度后体积收缩放出溶剂,重新投入使用。对分子量不同的各种物质进行浓缩实验的结果,溶质的分子量越高则浓缩的效果越好。用凝胶分离蛋白质、微生物等活性物质,可以避免加热等方法所产生副作用。Trank等人用凝胶来分离大豆蛋白质,与以往的酸凝法比较,质量、收率都较好。凝胶体积相变的研究方兴未艾。从基础研究的角度来看,如何制备结构可以完全表征的共聚胶试样及如何描述荷电基团间的相互作用,这是实验和理论方面的两个关键问题。利用凝胶是有待深入开发的领域。由于凝胶体系与生物机体在结构上的相似性,认识凝胶物质的运动规律对于理解生命过程的一些现象具有非常重要的意义。(华南理工大学材料科学研究所童真撰)