【TiCl4中钒杂质去除方法】
TiCl4是生产海绵钛和氯化法生产钛白的原料,钒是粗四氯化钛(未经提纯的TiCl4)的一种主要有害杂质,以VOCl3形式存在。用含VOCl3的TiCl4生产海绵钛,将增加产品的氧含量;钒是一种有色杂质,用含钒的带有颜色的TiCl4生产钛白,产品也会带上颜色。可见,无论是用于生产海绵钛还是钛白的原料四氯化钛,都必须预先经过除钒净化处理。粗TiCl4的精制提纯包括除去溶于其中气体杂质(如Cl2、N2等)、液体杂质(如SiCl4、VOCl3等)和固体杂质(如FeCl3、AlCl3等)以及细分散的固体悬浮物。除钒是精制TiCl4的一个重要工序。VOCl3的沸点(127℃)与TiCl4的沸点(136℃)接近。它们的挥发度差别不大(相对挥发度为1.22),采用一般的精馏方法很难将它们分离,各国均采用化学除钒法,工业生产已应用的只有如下4种方法。
1.铜除钒法。一般认为铜去除TiCl4中的VOCl3的机理是TiCl4与铜反应生成中间产物CuCl·TiCl3,后者还原VOCl3生成不溶性的VOCl2的沉淀:TiCl4+Cu=CuCl·TiCl3CuCl·TiCl3+VOCl3=VOCl2CuCl+TiCl↓(4铜还可与溶于TiCl4中的Cl2、AlCl3、FeCl3进行反应,当AlCl3在TiCl4中的浓度大于0.01%时,则会使铜表面钝化,阻碍除钒反应的进行。所以,当粗TiCl4中的AlCl3浓度较高时,一般要在除钒之前进行除铝。除铝的方法,一般是将用水增湿的食盐或活性炭加入TiCl4中进行处理,.AlCl3与水反应生成AlOCl沉淀:
AlCl3+H2O=AlOCl2HC1加入的水也可以使TiCl↓(4
发生部分水解生成TiOCl2,在有AlCl3存在时,可将TiOCl2重新转化为TiCl4:TiCl4+H2O=TiOCl2+2HClTiOCl2+AlCl3=AlOClTiCl↓(4由此可见,在进行脱铝时加入水量要适当,并应有足够的反应时间,以减少TiOCl2的生成量。
中国在生产海绵钛的初期,曾采用过铜粉除钒法,这种方法是间歇操作,铜粉耗量大,从失效的铜粉中回收TiCl4困难,劳动条件差。在20世纪60年代对铜除钒法进行了改进研究,研究成功了铜屑(或铜丝)气相除钒法,后来在工厂中应用。将铜丝卷成铜丝球装入除钒塔中,气相TiCl4(136~140℃)连续通过除钒塔与铜丝球接触,使钒杂质沉淀在铜丝表面上。当铜表面失效后,从塔中取出铜丝球,用水洗方法将铜表面净化,经干燥后返回塔中重新使用。采用该流程,因TiCl4中可与铜反应的AlCl3和自由氯等杂质已在除钒前除去,所以可减少铜耗量,净化lt TiCl4一般消耗铜丝2~4kg。铜对产品不会产生污染,除钒同时还可除去有机物等杂质,但失效铜丝的再生洗涤的操作麻烦,劳动强度大,劳动条件差,并产生含铜废水污染,也不便于从中回收钒,除钒成本高。所以,铜丝除钒法仅适合于处理含钒量低的原料和小规模生产海绵钛厂使用。2.铝粉除钒法。铝粉除钒的实质是TiCl3除钒。在有AlC3为催化剂的条件下,细铝粉可还原TiCl4为TiCl3,采用这种方法制备TiCl3-A1Cl3-TiCl4除钒浆液,把这种浆液加入到被净化的TiCl4中,TiCl3与溶于TiCl4中的VOCl3反应生成VOCl2沉淀: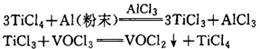
且AlCl3可将溶于TiCl4中的TiOCl2转化为TiCl4:
AlCl3+TiOCl2=TiCl4+AlOCl/p>铝粉除钒可将TiCl↓(4中的TiOCl2与AlCl3反应转化为TiCl4,有利于提高钛的回收率,除钒残渣易于从TiCl4中分离出来,并可从中回收钒。但细铝粉价格高,且是一种易爆物质,生产中要有严格的安全防护措施。除钒浆液的制备是一个间歇操作过程。3.硫化氢除钒法。硫化氢是一种强还原剂,它将VOCl3还原为VOCl2:2VOCl3+H2S=2VOCl22HCl+S硫化氢也可与TiCl↓(4
反应生成钛硫氯化物:TiCl4+H2S=TiSCl2+2HCl硫化氢与溶于TiCl4中的自由氯反应生成硫氯化物,为避免此反应的发生,在除钒前对粗TiCl4进行脱气处理以除去自由氯。经脱气的粗TiCl4预热至80~110℃,在搅拌下通入硫化氢气体进行除钒反应,并严格控制硫化氢的通入速度和通入量,以提高硫化氢的有效利用率和减少它与TiCl4的副反应。硫化氢除钒效果好,并同时可除去TiCl4中的Fe、Cr、Al等有色金属杂质和细分散的悬浮固体物。硫化氢的消耗与被处理的TiCl4中杂质含量和除钒条件有关,一般净化lt TiCl4要消耗1~2kg H2S。除钒残渣可用过滤或沉淀方法从TiCl4中分离出来。不过这种残渣的粒度极细,沉降速度小,沉降后的底流的液固比较大,除钒干残渣量一般是原料TiCl4重量的0.3%~0.35%,其中含钒量可达4%,残渣中的钛量占原料TiCl4中钛量的0.25%~0.30%。硫化氢除钒成本低,但硫化氢是一种具有恶臭味的剧毒和易爆气体,恶化劳动条件;除钒后的TiCl4饱和了硫化氢,必须进行脱气操作以去除溶于TiCl4的硫化氢,否则在其后的精馏过程中硫化氢会腐蚀设备,并与TiCl4反应生成钛硫氯化合物沉淀,引起管道和塔板的堵塞,并降低TiCl4的回收率。当原料TiCl4含钒量较高且附近又有硫化氢副产品的工厂时,可考虑选用硫化氢除钒法。美、日、英等国的某些海绵钛和钛白工厂采用硫化氢除钒法精制TiCl4。4.有机物除钒法。可用于除钒的有机物种类很多,一般选用油类(如矿物油或植物油等)。将少量有机物加入TiCl4中混合均匀,将混合物加热至有机物碳化温度(一般为120~138℃)使其碳化,新生的活性炭将VOCl3还原为VOCl2沉淀,或认为活性炭吸附钒杂质而达到除钒目的。粗TiCl4与适量有机物的混合物连续加入除钒罐进行除钒反应,并连续从除钒罐取出除钒的TiCl4(含有除钒残渣)加入高沸点塔的蒸馏釜中,定期从釜中取出残液进行过滤,过滤的滤液返回除钒罐进行除钒处理,分离出来的除钒残渣(含高沸点物)进行处理回收钒。TiCl4的精制过程可连续进行。有机物除钒操作简便,除钒效果好,但有如下问题需要研究解决:(1)除钒残渣易在容器壁上结疤,试验发现用于除钒的有机物种类不同,所生成的除钒残渣的性质也不相同。某些有机物(如液体石腊油)作为除钒试剂时,尽管它的加入量只有被处理的TiCl4重量的0.1%,但在除钒时却生成大量体积庞大的沉淀物,这种沉淀物呈悬浮状态,很难沉淀和过滤,将其蒸浓后的残液呈粘稠状,易在容器壁上粘结成疤。这种疤不仅严重影响传热,而且难以清除。这是因为这类有机物与TiCl4反应生成聚合性的残渣。使用这类有机物除钒,不仅会给操作带来许多困难,而且因生成渣量多而降低TiCl4的回收率,因此选择合适的有机物作为除钒试剂以生成不易结疤的除钒残渣,可以解决这个问题。试验发现,选用某些植物油和类似植物油的其它有机油类作为除钒试剂时,生成细分散的颗粒状的非聚合性残渣,这种残渣不粘稠,不易在容器壁上结疤,可用过滤方法将其从TiCl4中分离出来。除钒残渣量是原料TiCl4重量的0.4%~0.6%,残渣中的钛量是原料钛量的0.3%~0.5%,残渣中钒含量为2%左右。(2)除钒后的TiCl4在冷却时,有时会析出沉淀物,使冷凝器和管道发行堵塞。这是由于在除钒过程中生成的氧氯碳氢化合物(CHCl2COCl,CH2C1COCl)、光气(COCl2)与TiCl4反应生成一种固体加成物的缘故。在工艺和设备方面采取适当措施,便可防止这种固体加成物的生成。(3)在除钒过程中会有少量有机物溶于TiCl4中,这些有机物均是低沸点物,需在其后的精馏过程中加以除去。有机物廉价无毒,使用量少,除钒成本低;除钒同时可除去Cr、Sn、Sb、Fe及A1等有色金属杂质;除钒操作简便,精制TiCl4流程简化,可实现精制过程的连续操作,是一种比较理想的除钒方法。国外已广泛应用这种方法,中国对这种方法的研究还不充分,还有许多问题需在扩大试验中发现和解决。(北京有色金属研究总院邓国珠撰)